赛存速度再见证 | 干细胞冻存液系列产品获得美国FDA DMF备案
2023-12-20
赛存(北京)生物科技有限公司基于自研控冰冻存技术开发的干细胞冻存液系列产品(REF:CS-SC-N1;CS-SC-D1)已获得美国食品药品监督管理局(FDA)签发的DMF Ⅱ型备案(编号:039215;039214)受理函。

再次见证赛存速度,继2023年10月,赛存αβ-T细胞冻存液系列产品首次获得DMF备案之后,赛存干细胞冻存液系列产品于2023年12月顺利获得DMF备案,其中干细胞冻存液无DMSO款产品,还是全国首款获得第一类医疗器械备案的不含DMSO的冻存产品,双备案加持,开启安全冻存之路。赛存生物致力于打造国际领先的生物样本冷冻保存技术平台,为客户提供安全、高效、稳定的“精准冻存方案”。
FDA DMF备案受理函


使用DMF备案产品——降本增效,安全加倍
1.协助多种资质申请
DMF可用于支持新药研究申请(IND)、新药申请(NDA)、简化新药申请(ANDA)、另一个DMF或出口申请。
2.助力加速药物申报进程
使用具有DMF备案的产品,进行FDA临床申请或上市注册的监管备案文件时可直接引用产品的DMF编号,从而节约产品审查和注册时间,助力加速您的药物上市申报进程。
3.保护生产商商业机密
DMF持有者向所有使用产品的用户提供授权书,授权FDA在评审药品申请时对所涉及的DMF技术内容进行直接审查,而不需要将保密资料提供给用户,保护双方商业机密,更安全高效的促成商业合作。
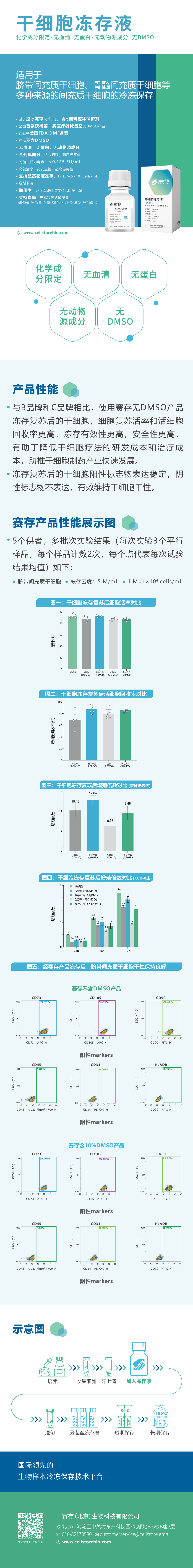
产品介绍——干细胞冻存液